KONSEP TERMODINAMIKA
KONSEP KONSEP TERMODINAMIKA
Termodinamika addalah ilmu yang menggambarkan usaha untuk mengubah kalor (perpindahan energi yang disebabkan perbedaan suhu) menjadi energi serta sifat-sifat pendukungnya
USAHA DALAM TERMODINAMIKA
w=f Δs
PROSES PROSES TERMODINAMIKA
Proses isobarik
Proses isobarik adalah perubahan keadaan gas pada tekanan tetap.
Persamaan keadaan isobarik:
Usaha yang dilakukan pada keadaan isobarik:
Proses isokhorik
Proses isokhorik adalah perubahan keadaan gas pada volume tetap.
Persamaan keadaan isokhorik:
Proses isotermis/isotermik
Proses isotermik adalah perubahan keadaan gas pada suhu tetap.
Persamaan keadaan isotermik:
Usaha yang dilakukan pada keadaan isotermik:
- Dari persamaan gas ideal
- Rumus umum usaha yang dilakukan gas:
maka:
karena bernilai tetap, maka:
Ingat integral ini!
maka persamaan di atas menjadi
maka menjadi:
Proses adiabatik
Proses adiabatik adalah perubahan keadaan gas dimana tidak ada kalor yang masuk maupun keluar dari sistem.
Persamaan keadaan adiabatik:
Tetapan Laplace:
karena , maka persamaan diatas dapat juga ditulis:
Usaha yang dilakukan pada proses adiabatik:
KAPASITAS KALOR
merupakan banyaknya kalor yang dibutuhkan untuk menaikkan suhu gas sebesar 1 derajat celsius dinyatakan dengan rumus
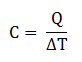
kapasitas kalor dibagi menjadi dua yaitu kapasitas kalor pada tekanan tetap cp dan kapasitas kalor pada volume tetap vp
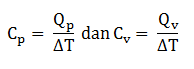
MESIN CARNOT DAN MESIN PENDINGIN
MESIN CARNOT
Mesin kalor bisa disebut juga Mesin Carnot. Mesin ini merupakan alat yang berfungsi mengubah energi panas menjadi energi mekanik. Sebagai contohnya, mesin motor ojek online tadi. Hasil pembakaran dari bahan bakar diubah menjadi energi gerak dalam mesin mobil.
Rangkaian mesin motor yang bergerak karena adanya energi panas dari hasil pembakaran bahan bakar.
Gambar di atas tadi merupakan piston yang ada pada mesin kendaraan yang menggunakan prinsip aliran kalor spontan.Mesin carnot memanfaatkan prinsip kaloryang mengalir dari suhu tinggi ke suhu rendah tanpa perlu melakukan usaha. Saat aliran kalor terjadi, panas yang mengalir diubah menjadi usaha, misalnya gerak. Konsep tersebutlah yang ditemukan oleh Nicolas Leonard Sadi Carnot.
Nicolas Leonard Sadi Carnot
Nah, supaya dapat menghasilkan usaha, mesin carnot perlu menjalani empat buah langkah yaitu 2 proses isotermal dan 2 proses adiabatik. Gambarannya itu seperti ini.
Siklus dalam mesin carnot
Pertama-tama, gas mengalami pemuaian isotermal. Pada saat ini, gas menyerap kalorQ1 dari reservoir suhu tinggi T1 dan melakukan usaha. Kemudian, gas mengalami pemuaian adiabatik. Pada proses ini, gas juga melakukan usaha.
Setelah melalui 2 proses pemuaian , gas mengalami kompresi/penyusutan isotermal. Gas membuang kalor Q2 ke reservoir suhu rendah T2. Pada proses ini, gas mendapatkanusaha. Akhirnya, di proses terakhir gas mengalami kompresi/penyusutan adiabatik. Pada proses ini, gas mendapatkan usaha kembali, dan kembali ke bentuk semula. Berhubung proses ini mengembalikan kondisi gas ke kondisi semula, maka siklus ini tidak mengalami perubahan energi dalam. Maka, persamaan termodinamikanya menjadi
Menurut Nicolas Carnot, mesin yang ideal adalah mesin yang sanggup mengubah seluruh panas menjadi usaha. Sayangnya, mesin ideal itu tidak pernah ada. Semua mesin tidak dapat mengubah seluruh panas menjadi usaha. Sebagian besar panas terbuang sia-sia. Sebagian lagi menjadi bunyi, getaran, atau asap dan hanya sebagian kecil yang menjadi usaha. Buktinya apa?
Hasil pembakaran mesin ada yang menjadi asap (sumber: giphy)
Oleh karena itu, ada konsep yang dikenal dengan efisiensi mesin Carnot. Efisiensi adalah perbandingan dari panas yang berubah menjadi usaha dengan panas yang diserap. Mudahnya begini, hasil bagi antara usaha yang dilakukan dengan kalor yang diserap. Rumusnya seperti ini.
Sementara di atas sudah disebutkan bahwa Q1 - Q2 =W, maka
Nah, karena Q1 = T1 dan Q2 = T2 , maka rumus di atas dapat juga berubah menjadi
MESIN PENDINGIN
Kalau kamu di dalam ruangan ber-AC, apa yang kamu rasakan?
Sejuk kan? Nah, coba kalau kamu berdiri di samping benda ini yang sebenarnya masih satu paket dengan AC yang kamu rasa sejuk itu, gimana rasanya?
Kompresor dan kondensor AC mengeluarkan hawa panas (sumber:artomorobarokahteknik.com)
Panas kan? Itu dia. Mesin pendingin seperti AC itu kebalikan dari mesin carnot. Mesin pendingin membuang kalor dari tempat dingin ke tempat panas dan membutuhkanusaha supaya proses tersebut bisa berjalan. Mesin pendingin membutuhkan usaha.
Kenapa perlu usaha? Ini karena proses pada mesin pendingin adalah tidak spontan. Usaha yang dibutuhkan untuk menjalankan mesin pendingin dapat dihitung menggunakan persamaan.
W = Q1 -Q2
Nah, seperti mesin carnot, mesin pendingin juga tidak ideal, alias tidak dapat mengubah semua usaha untuk membuang panas. Ada sebagian usaha yang dilakukan terbuang menjadi panas lagi, menjadi bunyi, dan atau menjadi getaran.
Jika mesin pendingin itu ideal, maka persamaan yang berlaku adalah
Nah, ketidakidealan mesin pendingin dapat dilihat dari koefisien performansi. Pada dasarnya, ini adalah “efisiensi versi mesin pendingin”. Koefisien performansi ditunjukkan dengan
Karena W = Q1 - Q2, maka
Atau, karena , maka
, maka
 , maka
, maka
Sekarang, kamu tahu kan kenapa angin keluaran dari AC terasa panas? Yups, karena mesin pendingin bertugas membuang panas yang ada di dalam ruangan ke luar ruangan.
CONTOH SOAL:
Mesin Carnot bekerja pada suhu tinggi 600 K, untuk menghasilkan kerja mekanik. Jika mesin menyerap kalor 600 J dengan suhu rendah 400 K, maka usaha yang dihasilkan adalah…. (UN Fisika 2009 P04 No. 18)
Jawab:
Diketahui:
T2 = 400 K
T1 = 600 K
T1 = 600 K
Ditanyakan: Wdihasilkan?
Wdihasilkan = . Wserap = = 200 J
Suatu gas memiliki volume awal 10 m3 dipanaskan dengan kondisi isobaris hingga volume akhirnya menjadi 25 m3. Jika tekanan gas adalah 2 atm, tentukan usaha luar gas tersebut! (1 atm = 1,01 x 105 Pa).
Jawab:
Diketahui:
V2 = 25 m3
V1 = 10 m3
P = 2 atm = 2,02 x 105 Pa
V1 = 10 m3
P = 2 atm = 2,02 x 105 Pa
Ditanyakan: W?
Isobaris → Tekanan Tetap, gunakan rumus W = P (ΔV)
W = P(V2 − V1)
W = 2,02 x 105 x (25 − 10) = 3,03 x 106 joule
Isobaris → Tekanan Tetap, gunakan rumus W = P (ΔV)
W = P(V2 − V1)
W = 2,02 x 105 x (25 − 10) = 3,03 x 106 joule













![{\displaystyle W=n\times R\times T\times [\ln V_{2}-\ln V_{1}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ebc1726c0b3fb85eb05f90053b50f6fb2ee2f441)





Comments
Post a Comment